
Une bonne mayonnaise !
Pourquoi peut-on réaliser une mayonnaise ?
Ci-dessous, une recette pour faire une bonne mayonnaise :
Mélangez un jaune d'œuf, un peu de sel, de poivre, de la moutarde et du vinaigre. Fouetter en versant peu à peu de l'huile : la mayonnaise doit peu à peu épaissir.
Et voilà, fin de l'article ?
Eh bien, non(2) !
Attardons-nous un peu sur le côté épaississant de la mayonnaise : qui en est responsable ? Qu'est-ce qui empêche ce mélange somme toute composé de produits en majorité liquides de finir en une espèce de blob flaqueux au fond de notre bol ?
Un indice, vous pouvez tout de suite enlever le sel, le poivre, la moutarde et le vinaigre de la liste des suspects : vous obtiendrez un résultat à peu près aussi épais en leur absence (cela dit, ledit résultat risque d'être fortement insipide).
Restent donc le jaune d'œuf et l'huile. Inutile de chercher à enlever l'un des deux de notre liste : c'est leur combinaison qui est responsable de l'aspect « mousseux » de notre mayonnaise.
Le phénomène observable ici est l'émulsion, qui se produit dans certaines conditions lorsqu'on met ensemble deux produits non-miscibles, c'est-à-dire qui ne peuvent pas se mélanger. Ici, nos deux produits sont l'huile et l'eau(3) ; cela dit, si vous mélangez de l'huile et de l'eau, vous obtiendrez un résultat assez peu probant :

En bref, rien de très épais.
Et c'est là qu'intervient le jaune d'œuf ! Car non content de contenir de l'eau, il apporte également un émulsifiant(4), qui a comme effet de stabiliser de fines gouttelettes de l'huile dans l'eau.

Les émulsifiants sont (souvent) des molécules linéaires, possédant une « tête » hydrophile lipophobe (c'est-à-dire qui « aime » l'eau et « n'aime pas » les graisses), et une « queue » lipophile hydrophobe (soit l'inverse : « aime » les graisses et pas l'eau). Ces molécules s'organisent alors pour avoir leur tête dans l'eau et leur queue dans l'huile, ce qui crée ces gouttelettes d'huile dans l'eau (puisque la sphère est la forme qui permet le plus de volume avec le moins de surface). Notons, pour un peu de vocabulaire : ces molécules sont nommées tensioactifs, et l'ensemble tensioactif-huile est nommé micelle(5).
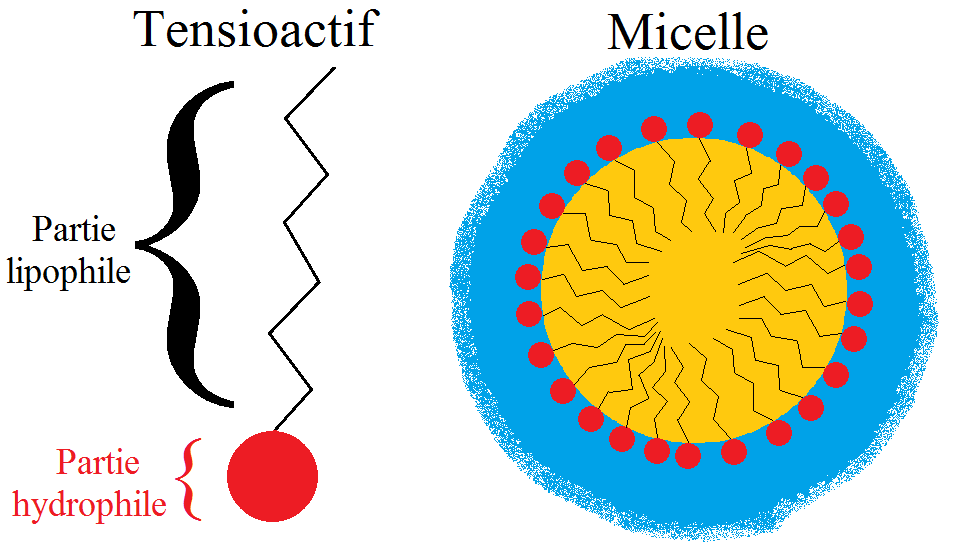
Et c'est ce mélange peu commun qui est à l'origine de la texture de notre mayonnaise !
Encore que, peu commun… Des émulsions, on en trouve ailleurs : la chantilly en est un exemple, à ceci près que dans ce cas, ce n'est pas deux liquides non miscibles, mais un liquide et un gaz : l'air(6) (l'émulsifiant ne fonctionne donc pas sur le même principe).
Notons enfin que les savons fonctionnent sur le même principe que les tensioactifs(7) : ils entourent les graisses avec leur partie lipophile, et les emportent avec l'eau qui les entraînera via leur partie hydrophile.
- (1) ↑ Étant moi-même un piètre cuisinier, vous auriez bien tort de suivre des conseils venant de moi…
- (2) ↑ Quelle surprise…
- (3) ↑ En effet, le jaune d'œuf, comme tout ce qui vient du vivant, contient de l'eau.
- (4) ↑ Pour les curieux, il s'agit de la lécithine de jaune d'œuf.
- (5) ↑ Comme le ver, oui.
- (6) ↑ Attention, les boissons gazeuses ne sont pas des émulsions ! Si il y a là aussi un mélange d'un liquide et d'un gaz, le gaz est dissous dans le liquide : il y a bel et bien miscibilité.
- (7) ↑ D'où le fonctionnement du shampoing au jaune d'œuf.